Atommodellek, az atom szerkezete, relatív tömeg, radioaktivitás
1. feladat
Mennyi a természetben előforduló klór átlagos relatív atomtömege, ha tudjuk izotópjainak az előfordulási százalékát:
$75,\!4 \%$ $ ^{35}_{17}\mathrm{Cl} $ és $24,\!6 \%$ $ ^{37}_{17}\mathrm{Cl} $.
$$\ \ $$
1. feladat
Mennyi a természetben előforduló klór átlagos relatív atomtömege, ha tudjuk izotópjainak az előfordulási százalékát:
$75,\!4 \%$ $ ^{35}_{17}\mathrm{Cl} $ és $24,\!6 \%$ $ ^{37}_{17}\mathrm{Cl} $.
2. feladat
Számítsd ki a természetes kálium izotópeloszlását ha tudjuk a kálium kétféle izotóp keveréke
39 és 41-es tömegszámú izotópja létezik és átlagos relatív atomtömege $ 39,\!1307 $.
$$\ \ $$
2. feladat
Számítsd ki a természetes kálium izotópeloszlását ha tudjuk a kálium kétféle izotóp keveréke
39 és 41-es tömegszámú izotópja létezik és átlagos relatív atomtömege $ 39,\!1307 $.
3. feladat
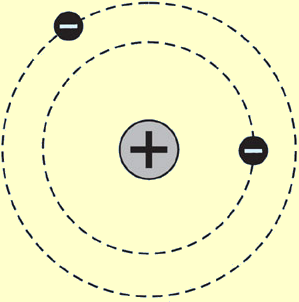
Hogyan nézett ki a Rutherford-féle atommodell? (Alább segítő kérdéseket találsz!)
- Mi volt a felfedezéshez vezető kísérlet neve?
- Mikor történt?
- Milyen kísérletet végzett Rutherford?
- Mit várt a korábbi modell alapján?
- Mi volt a tapasztalat?
- Rajzold le az új atommodellt?
$$\ \ $$
3. feladat
Hogyan nézett ki a Rutherford-féle atommodell? (Alább segítő kérdéseket találsz!)
- Mi volt a felfedezéshez vezető kísérlet neve?
- Mikor történt?
- Milyen kísérletet végzett Rutherford?
- Mit várt a korábbi modell alapján?
- Mi volt a tapasztalat?
- Rajzold le az új atommodellt?
4. feladat
Jellemezd az atomot felépítő elemi részecskéket! (Segítő kérdések alább!)
- Nevük, helyük az atomban
- Valódi tömegük, töltésük
- Relatív tömegük, töltésük
$$\ \ $$
4. feladat
Jellemezd az atomot felépítő elemi részecskéket! (Segítő kérdések alább!)
- Nevük, helyük az atomban
- Valódi tömegük, töltésük
- Relatív tömegük, töltésük
5. Karikázd be az egyetlen helyes választ!
A. Az atom tömegszámát megkapjuk
- a protonok és az elektronok számának összegeként
- a neutronok és az elektronok számának összegeként
- a protonok és a neutronok számának összegeként
- a protonok, a neutronok és az elektronok számának összegeként
- az izotópok tömegének átlagolásával
B. Melyik állítás igaz?
- Minden atommagban azonos számú proton és neutron van.
- A protonok száma minden atommagban nagyobb, mint a neutronok száma.
- Minden atommagban annyi neutron van, ahány elektron.
-
Ugyanabban az atomban a protonok és a neutronok
száma vagy egyenlő vagy a neutronok száma nagyobb, mint a protonok száma.
- Az atommagot a nukleonok építik fel.
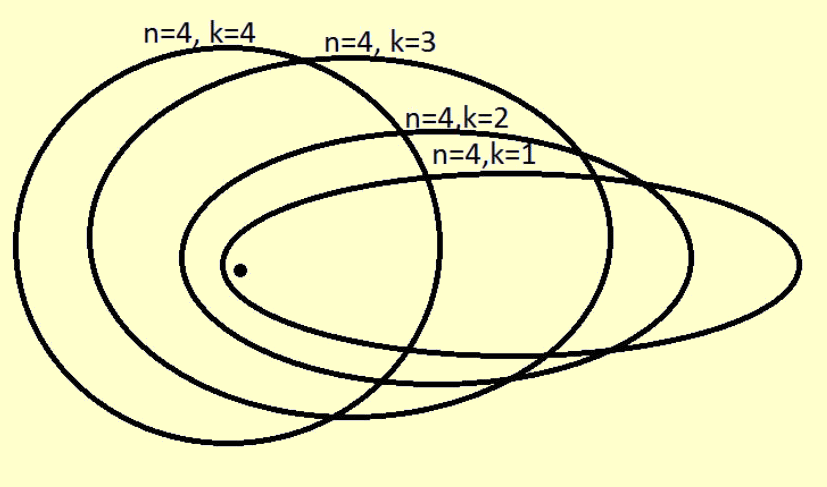 C. Sommerfeld szerint milyen alakúak lehetnek az elektronhéjak?
C. Sommerfeld szerint milyen alakúak lehetnek az elektronhéjak?
- Ellipszis és kör.
- Csak kör.
- Csak ellipszis.
- Tetszőleges alakúak.
- Bonyolult szimmetriájúak.
D. Dalton elmélete szerint mi az atomok legfontosabb jellemzője?
- Az atomok kisebb építőelemekből hozhatóak létre.
- Az atomok tovább nem bontható részecskék.
- Az atomok kémiai úton tovább bontható részecskék.
- Az atomok elektronból, protonból és neutronból állnak.
- Az atomok színe a legfontosabb jellemző.
$$\ \ $$
5. Karikázd be az egyetlen helyes választ!
A. Az atom tömegszámát megkapjuk
- a protonok és az elektronok számának összegeként
- a neutronok és az elektronok számának összegeként
- a protonok és a neutronok számának összegeként
- a protonok, a neutronok és az elektronok számának összegeként
- az izotópok tömegének átlagolásával
B. Melyik állítás igaz?
- Minden atommagban azonos számú proton és neutron van.
- A protonok száma minden atommagban nagyobb, mint a neutronok száma.
- Minden atommagban annyi neutron van, ahány elektron.
-
Ugyanabban az atomban a protonok és a neutronok
száma vagy egyenlő vagy a neutronok száma nagyobb, mint a protonok száma.
- Az atommagot a nukleonok építik fel.
 C. Sommerfeld szerint milyen alakúak lehetnek az elektronhéjak?
C. Sommerfeld szerint milyen alakúak lehetnek az elektronhéjak?
- Ellipszis és kör.
- Csak kör.
- Csak ellipszis.
- Tetszőleges alakúak.
- Bonyolult szimmetriájúak.
D. Dalton elmélete szerint mi az atomok legfontosabb jellemzője?
- Az atomok kisebb építőelemekből hozhatóak létre.
- Az atomok tovább nem bontható részecskék.
- Az atomok kémiai úton tovább bontható részecskék.
- Az atomok elektronból, protonból és neutronból állnak.
- Az atomok színe a legfontosabb jellemző.
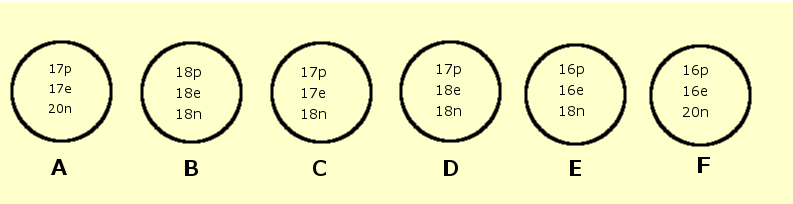
6. Tekintsük az alábbi összetételű nagybetűkkel jelölt részecskéket!
Válaszolj az alábbi kérdésekre! Ahol szükséges, használd a megfelelő nagybetűt!
- Hány kémiai elemről van szó?
- Van-e olyan részecske, amely nem jelölhet atomot? Ha igen melyik az, és miért? Ha nem, akkor azt indokold!
- Csoportosítsd az atomokat aszerint, hogy melyek izotópjai egymásnak!
- Izobárnak nevezzük az azonos tömegszámú részecskéket. Válaszd ki az izobár atomokat!
6. Tekintsük az alábbi összetételű nagybetűkkel jelölt részecskéket!
Válaszolj az alábbi kérdésekre! Ahol szükséges, használd a megfelelő nagybetűt!
- Hány kémiai elemről van szó?
- Van-e olyan részecske, amely nem jelölhet atomot? Ha igen melyik az, és miért? Ha nem, akkor azt indokold!
- Csoportosítsd az atomokat aszerint, hogy melyek izotópjai egymásnak!
- Izobárnak nevezzük az azonos tömegszámú részecskéket. Válaszd ki az izobár atomokat!
7. Esettanulmány
Olvasd el a szöveget, majd válaszolj a kérdésekre!
A radioaktív sugárzás a radioaktív anyag bomlásával jön létre. A természetben egyre kevesebb sugárzó anyag van,
és mennyiségük az állandó bomlás miatt folyamatosan csökken.
Igaz, ez a csökkenés lassú, évmilliók, évmilliárdok alatt valósul meg.
3,5 milliárd évvel ezelőtt már éltek egysejtűek a Földön,
pedig ekkor az $ ^{238}\mathrm{U}$ aktivitása 1,74-szer, az aktivitása 32-szer nagyobb volt a mainál.
A radioaktív bomlással mindkét uráncsalád eljut a radonig, amely nemesgáz lévén, kiszökhet a kőzetek repedésein keresztül.
A 235-ös tömegszámú uránizotóp felezési ideje nagyon kicsi, mindössze 4 s, a 238-as tömegszámú izotóp felezési ideje 4 nap.
Az utóbbiból származó radon jelen van a természetes vizekben és a légkörben.
Mátraderecskén mind a mai napig két gáz érkezik a földből a felszínre: a szén-dioxid és a radon.
Nagy mennyiségben a szén-dioxid is veszélyes gáz. Sajnos minden ősszel történik halálos baleset:
a must forrásakor fejlődő szén-dioxid gáz az óvatlan gazdák fulladásos halálát okozza.
Kis mennyiségben és nem belélegezve viszont értágító hatása lehet.
A radioaktív és az izotóp szót hallva az emberek megijednek, félnek. Pedig a felmérések azt mutatják, hogy közepes radontartalmú levegőben
élő nők között kevesebb a rákos megbetegedés, mint ott, ahol átlagos a környezet radontartalma.
A férfiaknál a dohányzás elfedi a jótékony hatást.
A radioaktív nyomjelzés felfedezése Hevesy György magyar származású, Nobel-díjas tudós nevéhez fűződik.
1923-ban a növények anyagcseréjének vizsgálatára használt sugárzó-izotópokat. Később a
$ ^{32}\mathrm{P}$ -izotóppal a foszforanyagcserét tanulmányozta állatok szervezetében.
- Miben különbözik egymástól a $ ^{235}\mathrm{U}$ és a $ ^{238}\mathrm{U}$ -atom?
- Az atomnak melyik része alakul át a radioaktív bomlás során?
- Honnan származik a légkörben lévő radon?
- Hol található a periódusos rendszerben a radon?
- Miért csökken a természetben található radioaktív anyagok mennyisége?
- Milyen gázok törnek a felszínre Mátraderecskén?
- Ki volt Hevesy György?
$$\ \ $$
7. Esettanulmány
Olvasd el a szöveget, majd válaszolj a kérdésekre!
A radioaktív sugárzás a radioaktív anyag bomlásával jön létre. A természetben egyre kevesebb sugárzó anyag van,
és mennyiségük az állandó bomlás miatt folyamatosan csökken.
Igaz, ez a csökkenés lassú, évmilliók, évmilliárdok alatt valósul meg.
3,5 milliárd évvel ezelőtt már éltek egysejtűek a Földön,
pedig ekkor az $ ^{238}\mathrm{U}$ aktivitása 1,74-szer, az aktivitása 32-szer nagyobb volt a mainál.
A radioaktív bomlással mindkét uráncsalád eljut a radonig, amely nemesgáz lévén, kiszökhet a kőzetek repedésein keresztül.
A 235-ös tömegszámú uránizotóp felezési ideje nagyon kicsi, mindössze 4 s, a 238-as tömegszámú izotóp felezési ideje 4 nap.
Az utóbbiból származó radon jelen van a természetes vizekben és a légkörben.
Mátraderecskén mind a mai napig két gáz érkezik a földből a felszínre: a szén-dioxid és a radon.
Nagy mennyiségben a szén-dioxid is veszélyes gáz. Sajnos minden ősszel történik halálos baleset:
a must forrásakor fejlődő szén-dioxid gáz az óvatlan gazdák fulladásos halálát okozza.
Kis mennyiségben és nem belélegezve viszont értágító hatása lehet.
A radioaktív és az izotóp szót hallva az emberek megijednek, félnek. Pedig a felmérések azt mutatják, hogy közepes radontartalmú levegőben
élő nők között kevesebb a rákos megbetegedés, mint ott, ahol átlagos a környezet radontartalma.
A férfiaknál a dohányzás elfedi a jótékony hatást.
A radioaktív nyomjelzés felfedezése Hevesy György magyar származású, Nobel-díjas tudós nevéhez fűződik.
1923-ban a növények anyagcseréjének vizsgálatára használt sugárzó-izotópokat. Később a
$ ^{32}\mathrm{P}$ -izotóppal a foszforanyagcserét tanulmányozta állatok szervezetében.
- Miben különbözik egymástól a $ ^{235}\mathrm{U}$ és a $ ^{238}\mathrm{U}$ -atom?
- Az atomnak melyik része alakul át a radioaktív bomlás során?
- Honnan származik a légkörben lévő radon?
- Hol található a periódusos rendszerben a radon?
- Miért csökken a természetben található radioaktív anyagok mennyisége?
- Milyen gázok törnek a felszínre Mátraderecskén?
- Ki volt Hevesy György?

 C. Sommerfeld szerint milyen alakúak lehetnek az elektronhéjak?
C. Sommerfeld szerint milyen alakúak lehetnek az elektronhéjak?